

发布时间:2025-01-10来源:黄清育研究组
砷在自然界中广泛存在,其暴露可导致非酒精性脂肪肝(NAFLD)等肝脏疾病。组蛋白修饰是一种重要的表观遗传机制,通过调控相关基因表达在肝脏脂质代谢过程中发挥重要作用,但其在砷暴露诱发NAFLD中的作用机制却仍不明确。
中国科学院城市环境研究所环境健康研究组(黄清育团队)通过分析无机砷(NaAsO2)在大鼠肝脏中的代谢及其对S-腺苷甲硫氨酸(SAM)、组蛋白甲基化修饰的影响,探讨了砷甲基化和组蛋白修饰共调控在砷暴露导致NAFLD中的作用机制。结果发现,砷暴露导致大鼠肝脏脂质蓄积,并上调脂质代谢相关基因Fabp1、Srebf1和Apoc3的表达。此外,组蛋白甲基化(H3K9me1/2)水平降低;无机三价砷(iAsIII)在肝脏中主要代谢为有机砷DMA,且SAM水平下降。体外实验显示,补充SAM可部分恢复H3K9me1/2水平,并下调Fabp1、Srebf1和Apoc3表达,从而有效缓解砷暴露诱导的肝细胞脂质蓄积。综上,砷可通过其自身甲基化代谢消耗肝脏中的SAM,从而抑制H3K9me1/2,导致Fabp1、Srebf1和Apoc3过表达,最终诱导肝脏脂质蓄积,促进NAFLD的发生发展。该研究揭示了SAM介导的组蛋白甲基化在砷诱导NAFLD中的作用,可为环境砷暴露所致肝脏疾病的预防和干预提供依据。
相关研究成果以Arsenic Exposure Triggers Nonalcoholic Fatty Liver Disease through Repressing S-Adenosylmethionine-Dependent Histone Methylation in Rats为题发表在环境领域权威期刊Environmental Science & Technology。城市环境研究所与福建农林大学联合培养硕士生鲁璐和研究实习员华炜桢为共同第一作者,卢艳阳助理研究员和黄清育研究员为共同通讯作者。该研究得到了国家自然科学基金项目(22076179, 22076157, 21677142),及福建省自然科学基金(2022J06033, 2023J01224)的资助。
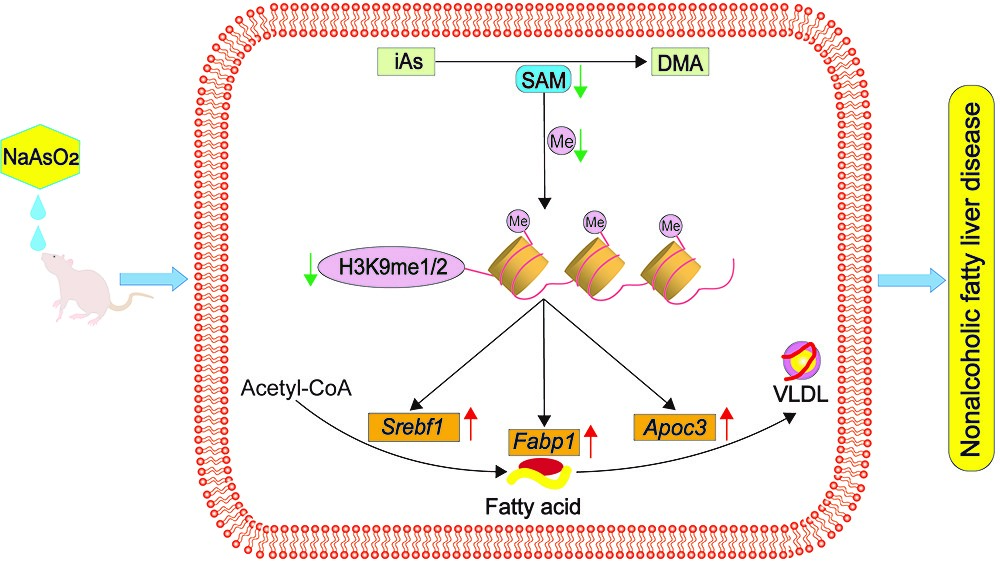
砷暴露通过抑制SAM依赖的组蛋白甲基化诱导NAFLD
附件下载: